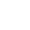Definiția pH-metrului
Un pH-metru se referă la un instrument utilizat pentru a determina valoarea pH-ului unei soluții. pH-metrul funcționează pe principiul unei baterii galvanice. Forța electromotoare dintre cei doi electrozi ai bateriei galvanice se bazează pe legea lui Nerns, care nu este legată doar de proprietățile electrozilor, ci și de concentrația ionilor de hidrogen din soluție. Există o relație corespunzătoare între forța electromotoare a bateriei primare și concentrația ionilor de hidrogen, iar logaritmul negativ al concentrației ionilor de hidrogen reprezintă valoarea pH-ului. pH-metrul este un instrument analitic comun, utilizat pe scară largă în agricultură, protecția mediului și industrie. PH-ul solului este una dintre proprietățile de bază importante ale solului. Factori precum temperatura și tăria ionică a soluției care urmează să fie testată ar trebui luați în considerare în timpul măsurării pH-ului.
Principiul pH-metrului
pH-ul este definit ca logaritmul negativ al concentrației de ioni de hidrogen din soluția apoasă. Deși pare complicat, în termeni foarte simpli, pH-ul este un număr utilizat pentru a cuantifica aciditatea sau alcalinitatea unei soluții. Numărul indică numărul de ioni de hidrogen pe care o anumită substanță îi poate elibera în soluție. În intervalul pH-ului, un pH de 7 este considerat neutru. Soluțiile cu un pH de 0-7 sunt considerate acide, iar soluțiile peste 7 până la 14 sunt numite soluții alcaline. În sistemele biologice, pH-ul este critic. Datorită pH-ului atent ajustat, majoritatea biomoleculelor din corpul nostru pot îndeplini funcții excelente. Chiar și într-un sistem experimental, pH-ul necesar trebuie menținut pentru a obține rezultate precise. Prin urmare, în experimentele biologice, se utilizează un dispozitiv numit pH-metru pentru a monitoriza cu atenție pH-ul.
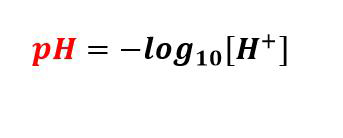
pH-metrul este un electrod sensibil la pH care măsoară activitatea ionilor de hidrogen dintr-o soluție și transmite aceste informații. Dispozitivul este alcătuit din două tuburi de sticlă, fiecare conținând un electrod, un electrod de referință și un electrod senzor. Electrodul de referință este fabricat dintr-o soluție saturată de KCl, în timp ce electrodul senzor conține o soluție tampon cu un pH de 7, iar firul de argint acoperit cu clorură de argint este imersat în aceste două soluții. La capătul electrodului senzor se află un bec fabricat din sticlă poroasă acoperită cu silice și sare metalică.
Pentru a măsura pH-ul soluției, pH-metrul este scufundat în soluție. După ce becul electrodului senzorului intră în contact cu soluția, ionii de hidrogen din soluție vor înlocui ionii metalici de pe bec. Această substituție a ionilor metalici determină curgerea curentului în firul metalic, care este citit de un voltmetru.
pH-metrul este unul dintre cele mai utilizate echipamente în laboratoarele biologice. Analizați în mod curent pH-ul soluțiilor tampon, al soluțiilor și al reactivilor pentru a vă asigura că sunt îndeplinite condițiile experimentale. Pentru a asigura citiri precise, echipamentul trebuie calibrat periodic.
Aplicarea detectorului de pH-metru
Aplicarea detectorului de pH-metru în procesul de epurare a apelor uzate menajere

Aplicarea pH-metrului în tratarea apelor uzate prin galvanizare

Aplicarea pH-metrului online în industrie

Calibrarea pH-metrului
Data publicării: 15 decembrie 2021